Quote:
Originariamente inviata da zicchinet
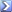
L'azione alcalina di iodio sul veleno per roditori Varfarina, C 19 H 16 O 4 (PM 308.34) consiste nella formazione di una mole di Iodoformio, CHI 3 , per ogni mole di Varfarina. L'analisi della Varfarina è quindi basata sulla reazione tra CHI 3 e Ag + : CHI 3 + 3 Ag + + H 2 O → 3 AgI (s) + 3 H + + CO
Il CHI 3 prodotto da un campione di 12,82 g è stato trattato con 25 mL di AgNO 3 0.0325 M e l'eccesso di Ag + è stato successivamente titolato con 3.45 mL di KSCN 0.06535 M .
Calcolare la percentuale di Varfarina nel campione.
|
Risultato: 4.69%
Esecuzione: Dalla titolazione con KSCN si ricava la quantitá di Ag+ in eccesso che non ha reagito con lo CHI3: la M di KSCN per il volume dá le mmol, quindi i meq, che corrispondono ai meq di Ag+ in eccesso. Dalla M di AgNO3 per il volume utilizzato si ricavano i meq totali di AgNO3: a questi si sottraggono quelli in eccesso che hanno regito con il KSCN. Si ottengono cosí i meq di Ag+ che hanno reagito con CHI3. Questi diviso 3 (essendo il rapporti 1:3), danno i meq di CHI3 = mmol CHI3 = mmol di Varfarina (rapporto 1:1 di reazione). Le mmol per il PM danno i mg di Varfarina. I mg diviso i mg di campione per 100, danno la % di Varfarina nel campione.